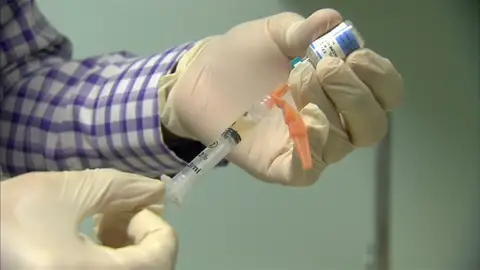
Salud
España es líder en investigación oncológica, pero el paciente tarde una media de dos años en acceder al fármaco
Nuestro país tarda una media de dos años en aprobar fármacos contra el cáncer ya validados en Europa.

Publicidad
Nuestro país es puntero en investigación médica. Es el primer país de Europa por número de pacientes en ensayo clínico y el tercero a nivel mundial, solo por detrás de Estados Unidos y China.
Algo muy positivo pero que pierde valor debido a la demora que tiene el paciente a la hora de acceder a los fármacos. Y es que los avances en los tratamientos médicos se desvalorizan cuando los pacientes no pueden disponer de ellos en un plazo breve desde su descubrimiento. Y esto es precisamente lo que sucede en España con las terapias contra el cáncer, donde un medicamento oncológico tarda dos años en ser aprobado por el Sistema Nacional de Salud después de ser valorado de manera positiva por la Agencia Europea del Medicamento, según indica la Asociación Española de Investigación sobre el Cáncer.
El tiempo medio desde que un compuesto antitumoral recibe el aprobado de la Agencia Europea del Medicamento hasta que tiene la aprobación para reembolso del Sistema Nacional de Salud ha aumentado desde los 395 días en 2018 a los 721 en 2023. "España es uno de los países que más ha empeorado el retraso a los medicamentos oncológicos innovadores en los últimos cinco años, y estos retrasos tienen consecuencias reales para los pacientes", relata la doctora Marisol Soengas, presidenta previa de Aseica.
Proceso complejo
El proceso para financiar un medicamento en nuestro país resalta por su complejidad. Primero, la farmacéutica debe presentar una solicitud de comercialización a la Agencia Española de Medicamentos y Productos Sanitarios. A continuación, el medicamento entra en negociación de precio y financiación a través de la Dirección General de Cartera Común de Servicios del Sistema Nacional de Salud y Farmacia y la Comisión Interministerial de Precios de los Medicamentos y Productos Sanitarios, un órgano en el que participan los Ministerio de Sanidad, Industria y Economía y las comunidades autónomas. Después, ya puede pasar a la cartera de servicios del Sistema Nacional de Salud, pero también puede haber otros retrasos puesto que las comunidades e incluso los hospitales pueden abrir nuevas negociaciones.
Las cifras van en aumento
Las cifras van en aumento cada año. El informe anual "Indicadores de acceso a terapias innovadora en Europa 2023 (W.A.I.T)" revelaba en 2024 que el tiempo medio de demora llegaba a los 661 días, un 5,1% más que en 2023. Un mes más de espera y lo que significaba casi cuatro veces más que los 180 días establecidos tanto en la legislación europea como en la nacional. En 2019 la demora media era de 414 días. Desde entonces las sociedades científicas y los colegios de médicos han venido reclamando una reducción de esos tiempos de espera interviniendo, por ejemplo, en los Informes de Posicionamiento Terapéutico en los que se valora la incorporación de innovaciones al Sistema Nacional de Salud.
Si en lugar de tener en cuenta la fecha de la autorización europea (que es única para toda Europa y por eso se toma como referencia) contabilizamos el tiempo desde que la compañía farmacéutica solicita su comercialización en cada estado, el tiempo en España se reduce hasta los 551 días de media.
Enfermedades raras
La situación de los fármacos para las enfermedades raras es similar. En España están disponibles sólo la mitad de los aprobados. De ellos, el 44% tienen alguna restricción de uso, lo que significa que sólo uno de cada tres medicamentos huérfanos llega a los pacientes sin trabas. Los tiempos de demora también son dilatados, aunque desde el último informe se aprecia mejoría. Están, de media, en los 704 días desde la aprobación europea hasta su incorporación al Sistema Nacional de Salud.
Las cifras muestran una gran disparidad entre los países europeos, aunque también es dispar el sistema de aprobación de cada estado. Alemania, por ejemplo, que tiene los mejores datos, incorpora las innovaciones según son aprobadas por la EMA y abre un periodo de tres meses de valoración y negociación con la empresa fabricante. Eso hace que su demora de financiación se sitúe en los 126 días.
Más Noticias
Síguenos en nuestro canal de WhatsApp y no te pierdas la última hora y toda la actualidad de antena3noticias.com
Publicidad